약리작용 및 기전
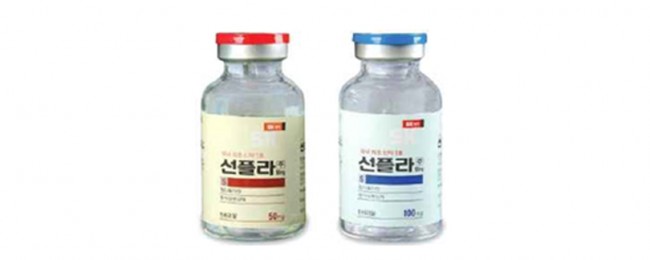
선플라주 (헵타플라틴)는 백금착체 항암제로, 암세포에 확산 침투하여 성분 중의 백금이 암세포의 핵 내에 존재하는 DNA 이중나선에 들어가 cross-linkage를 형성한다. 이를 통해서 DNA 복제과정을 억제하며 세포주기 중 S-phase에 주로 작용하여 암세포의 성장과 증식을 억제함으로써 항암 효과를 나타낸다. 선플라는 방광암, 폐암, 고환암, 난소암, 소아 임파종 등에 사용된다. 선플라는 제1세대 백금착체 항암제인 시스플라틴 (Cisplatin) 보다 항암 효과 (특히 위암에 대해서)가 강하며 제2세대 백금착체 항암제인 카보플라틴 (Carboplatin) 보다 부작용이 약하다.
연구개발 과정 및 최종 결과
제2세대 백금착체 항암제인 carboplatin이 개발된 이후 일본 및 미국의 제약회사들은 새로운 백금착체 (Platinum complex) 화합물 개발을 진행했다. 그러나 이들 화합물 모두가 독성은 감소되었으나 항암 효과가 이 계열 대표 약물인 cisplatin에 비해 낮았다. 따라서 cisplatin보다 강력한 항암 효과를 보유하면서, 독성이 감소되고 cisplatin 내성 암에도 유효한 새로운 화합물 개발을 목표로 SK케미칼 생명과학연구소 신약개발팀은 1990년 5월 제3세대 백금착체 항암제 개발을 시작했다.
120여 개의 신물질에 대한 drug design, 합성, 약효 및 독성 검색을 거쳐 1991년 12월 신약후보 물질로 SKI-2053R (헵타플라틴)을 선정, 실험동물에 대한 전임상시험 과정을 마치고 1993년 8월 국내 개발 신약으로는 최초로 임상시험 허가를 받았다.
1993년 10월부터 약 1년간 항암 치료에 필요한 용법 용량을 결정하기 위한 환자를 대상으로 한 제1상 임상시험을 서울대병원에서 성공리에 마치고 이어서 1995년 1월부터 항암 효과 평가를 위한 제2상 전기 임상시험을 위암, 폐암, 자궁경부암 및 두경부암 등에서 실시하였다.
제2상 임상시험 중 위암에 대한 평가 결과, 항암 효과는 기존의 제2세대 백금착체 항암제인 cisplatin과 동등 이상의 효과를 보인 반면 부작용은 훨씬 적은 빈도와 강도로 나타났다.
이 같은 결과를 바탕으로 1997년 6월부터 진행성 위암에 대하여 선플라 (헵타플라틴)와 병용 항암제 5-Fluorouracil을 함께 투여하는 복합 화학 요법에 의한 제2상 후기 임상시험을 실시하였다. 서울대병원을 중심으로 8개 병원에서 다기관 공동연구 방식으로 임상시험에 착수하여 1999년 1월 제2상 임상시험을 완료하였고 3월 초에 8개 임상병원의 임상시험 심사위원회 (IRB)의 심의를 모두 통과하였다. 이후 식품의약품안전처에 의한 임상병원 및 SK제약에 대한 심사가 실시되었고 6월 3일 중앙약사심의위원회를 통과하여 최종 발매 허가를 획득하였다. 이 모든 과정에 정부 연구비 13.6억 원을 포함 총 연구개발 비용 81억 원이 투입되었다.
SK케미칼 홈페이지: https://www.skchemicals.com/ls/kor/main.do
약학정보원: http://www.health.kr/searchDrug/result_drug.asp?drug_cd=A11A1890A0145